Diferença chave: Uma ligação iônica é uma ligação química entre dois átomos dissimilares (isto é, um metal e um não-metal) nos quais um átomo fornece um elétron para outro. Uma ligação covalente é outra ligação química forte. Ocorrem átomos semelhantes (isto é, dois não-metais). Em uma ligação covalente, os dois átomos se juntam para compartilhar o elétron, em vez de um átomo tomando um elétron de outro.
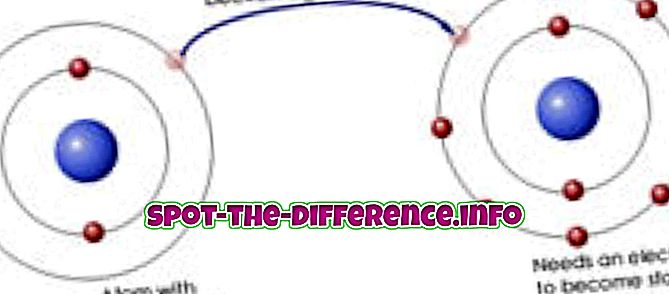
Uma ligação iônica é uma ligação química entre dois átomos diferentes (isto é, um metal e um não-metal) nos quais um átomo libera um elétron para outro. Portanto, ambos os átomos se tornam íons, como um átomo tem um elétron a menos, enquanto o outro tem um extra. O íon metálico que perdeu um elétron tem uma carga positiva. O íon não metálico que ganhou um elétron tem uma carga negativa. Como os opostos se atraem, esses íons são fortemente atraídos um pelo outro, tão fortemente que se tornam ligados.
Os compostos iônicos estão geralmente na forma de sólidos, isto é, sais. Eles são altamente solúveis em água e têm um alto ponto de fusão. Quando eles estão na água, eles também têm uma alta condutividade elétrica.

A liga�o covalente inclui muitos tipos de interac�o, incluindo liga�o-σ, liga�o-π, liga�o metal-metal, interac�es ag�ticas e liga�es de dois electr�s de tr� centros. Quando um átomo tem um elétron em sua camada externa e outro átomo exige que um elétron preencha sua camada externa, os dois átomos se juntam para compartilhar o elétron. Portanto, ambos os átomos acabam tendo uma camada exterior completa e correspondentemente uma configuração eletrônica estável.
As ligações químicas são feitas de modo que o átomo possa ter um invólucro externo completo, pois um invólucro externo completo significa uma configuração eletrônica estável. Em uma ligação iônica, quando o átomo de metal tem um único elétron em sua camada externa e o não-metal precisa de um elétron para completar sua camada externa, o átomo de metal dá seu elétron para o não-metal. Da mesma forma, na ligação covalente, eles compartilham o elétron igualmente.
Ligação iônica | Ligação covalente | |
Definição | Uma ligação química entre dois átomos dissimilares em que o átomo desiste de um elétron para outro. | Uma ligação covalente é uma ligação química que envolve o compartilhamento de elétrons entre dois átomos semelhantes. |
Ocorrência | Um metal e um não-metal | Dois não-metais |
Polaridade | Alto | Baixo |
Forma, de, molécula | Nenhuma forma definida, estruturas de treliça | Forma definitiva |
Condutividade elétrica | Alto | Geralmente nenhum |
Condutividade térmica | Alto | Geralmente baixo |
Ponto de fusão da substância | Varia, mas geralmente maior que os compostos covalentes | Varia, mas geralmente menor que os compostos iônicos |
Ponto de ebulição da substância | Alto | Varia, mas geralmente menor que os compostos iônicos |
Solubilidade em Água | Alto | Varia, mas geralmente menor que os compostos iônicos |
Estado da substância à temperatura ambiente | Geralmente sólido | Sólido, líquido, gás |