Diferença chave: Difusão é o processo pelo qual as moléculas se movem e viajam de um lugar para outro sem exigir movimento em massa. A efusão é o processo pelo qual as moléculas viajam através de um orifício de um local de alta concentração para baixa concentração.
Os termos difusão e efusão são comumente usados em muitas ciências, como química, física e biologia. Em química, esses dois termos são duas propriedades dos gases. Estes dois são confusos para muitas pessoas que estão aprendendo apenas o básico dos gases e suas propriedades. Difusão e Efusão são dois termos diferentes que significam duas coisas diferentes e não devem ser usados de forma intercambiável. Difusão refere-se à capacidade dos gases se misturarem, enquanto a efusão se refere à capacidade do gás de atravessar um pequeno orifício. A difusão também é usada em sociologia, economia e finanças para se referir à difusão de pessoas, idéias e valores.
A difusão é o processo pelo qual as moléculas se movem e viajam de um lugar para outro sem exigir movimento em massa. A difusão resulta em moléculas movendo-se ou misturando apenas usando energia cinética. A palavra "difusão" é derivada da palavra latina "diffundere" que significa "espalhar-se". Na difusão, as moléculas estão em constante estado de movimento e, quando impulsionadas pela energia cinética ou térmica, tendem a se misturar com outras moléculas, resultando em uma mistura inseparável. Vamos dar uma abordagem prática, um contêiner é dividido em seções A & B usando uma partição sólida; a primeira seção é preenchida com água, enquanto a segunda seção é preenchida com tinta vermelha. Agora, quando a divisória é levantada, o corante e a água tentam preencher todo o recipiente. Então, o corante lentamente mancha a água vermelha, sendo essa a difusão.
A difusão faz com que as moléculas mudem de uma área de concentração mais alta para uma área de concentração mais baixa, resultando na mistura de todas as moléculas. A difusão pára quando todas as moléculas estão uniformemente espalhadas. A difusão não se limita à água e funciona melhor em estados gasosos, onde as moléculas têm mais energia e capacidade de se misturar com outras moléculas. Existem duas abordagens para a difusão: fenomenológica e atomística. De acordo com a abordagem fenomenológica, as moléculas viajam de regiões de maior concentração para regiões de menor concentração. Na abordagem atomística, considera-se que a difusão ocorre devido ao passeio aleatório das partículas difusoras, no qual a difusão é impulsionada pela energia térmica, fazendo com que elas se misturem. Difusão desempenha um papel importante na criação de minerais, nutrientes e energia que são exigidos pelo organismo.

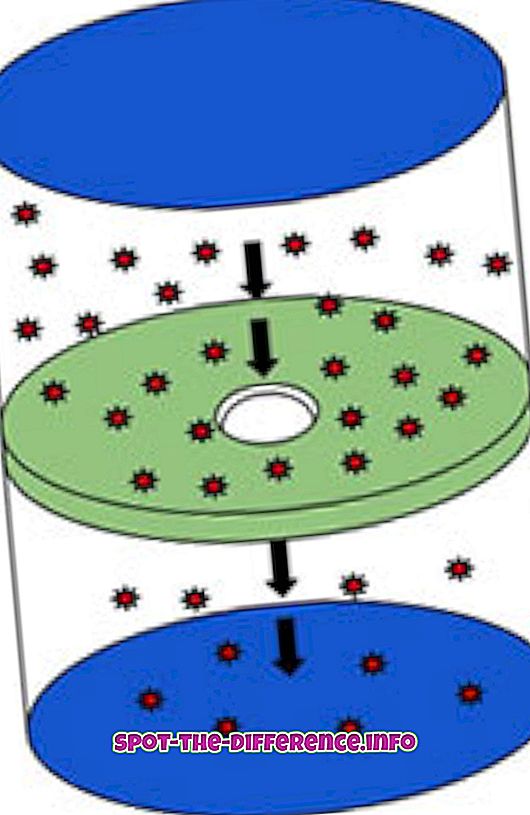
A efusão é o processo pelo qual as moléculas viajam através de um orifício de um local de alta concentração para baixa concentração. O processo descreve a capacidade do gás de atravessar um pequeno buraco sem colisões entre moléculas. Isso ocorre quando o diâmetro do furo é consideravelmente menor que o caminho livre médio das moléculas. O caminho livre médio é a distância média percorrida por uma partícula em movimento entre colisões sucessivas. Um exemplo prático disso seria encher uma garrafa com uma garrafa de fumaça e furar um pequeno orifício na garrafa, a fumaça que começa a sair do buraco é considerada uma efusão.
De acordo com o químico escocês Thomas Graham, que criou a fórmula para medir a efusão, criou uma Lei de Graham que determina a rapidez com que o gás viajará e como ele pode ser medido. De acordo com a Lei de Graham, a taxa na qual o efluente dos gases é dependente do seu peso molecular. O gás com um peso molecular menor será mais rápido do que um gás com um peso molecular mais alto. A efusão é calculada medindo quantas moléculas passam pelo orifício em um segundo. Similarmente, na termodinâmica, a taxa de efusão de um gás é inversamente proporcional à raiz quadrada da massa de suas partículas.